
《世界临床药物》

在生物创新药的研发与投资领域,创新药物的研发和审评是以临床价值为导向的。在当前生物创新药行业处在高速增长的发展窗口期,创新生物药企的内在价值,则需要可靠的研发成果来印证。
作为AACR(美国癌症研究协会)、ASCO(美国肿瘤学会)等国际顶级肿瘤学术盛会的常客,创新药头部企业亚盛医药-B(06855)再度携五个原创新药的六项最新临床前进展参加AACR大会,向国际学界展现自身的全球创新研发成绩。
智通财经APP了解到,4月14日,亚盛医药-B(06855)宣布,公司在刚刚举行的2022年美国癌症研究协会(AACR)年会上公布了六项最新临床前研究结果,包括细胞凋亡管线重要品种Bcl-2抑制剂lisaftoclax(APG-2575)、MDM2-p53 抑制剂alrizomadlin(APG-115),FAK抑制剂APG-2449,EED抑制剂APG-5918,KRAS抑制剂APG-1842五个在研品种。
AACR年会是全球历史最悠久、规模最大的肿瘤研究学术会议之一。会议关注高质量肿瘤研究及创新的各个方面,是全球肿瘤研究的焦点,将汇集肿瘤领域的最前沿的研究成果。
亚盛医药首席医学官翟一帆表示:“在今年的AACR年会上,我们展示了以解决患者未满足的临床需求导向下的进一步探索,为公司多个重要品种与其他靶点、其他机理药物的联合治疗提供了充分的科学支持。特别可圈可点的是,我们的MDM2-p53 抑制剂APG-115 共有三项研究获得展示,在呈现多种治疗潜力的同时,还有望进一步揭示新的作用机制;EED抑制剂APG-5918同样呈现较大的开发潜力等。我们将继续推进相关更深入的临床研究,早日造福患者。”
亚盛医药在本届AACR年会上展示了以下壁报信息:
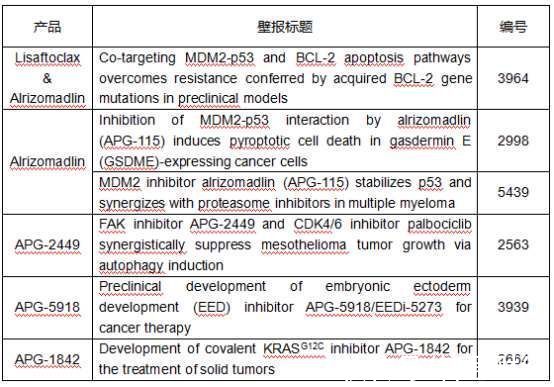
Co-targeting MDM2-p53 and BCL-2 apoptosis pathways overcomes resistance conferred by acquired BCL-2 gene mutations in preclinical models
双重靶向MDM2-p53和BCL-2细胞凋亡通路可克服临床前模型中获得性BCL-2基因突变导致的耐药
摘要编号:3964
研究背景:
BCL-2抑制剂venetoclax在慢性淋巴细胞白血病患者中具有显著疗效,但它的临床效益受到获得性BCL-2基因突变带来的耐药性限制。在获得性突变中,BH3结合基序邻近的突变(如G101V、D103E和V156D)对BCL-2与BH3-only促死亡蛋白和BH3模拟物(如venetoclax)的结合影响最大。因此,为这一尚未满足的临床需求寻求新的治疗手段是非常重要的。
结论:
该研究表明, APG-2575(lisaftoclax)联合APG-115(alrizomadlin)可协同抑制携带BCL-2突变的RS4:11细胞的增殖及其在活体异种移植瘤模型中的生长。联合靶向BCL-2和MDM2-p53细胞凋亡通路为克服由BCL-2突变所导致的获得性耐药性提供了一种有效的全新策略。
Inhibition of MDM2-p53 interaction by alrizomadlin (APG-115) induces pyroptotic cell death in gasdermin E (GSDME)-expressing cancer cells
Alrizomadlin (APG-115) 对于MDM2-p53相互作用的抑制可诱导gasdermin E (GSDME) 阳性癌细胞的焦亡性细胞死亡
摘要编号:2998
研究背景:
MDM2-p53抑制剂APG-115(alrizomadlin)是一种可诱导tp53野生型癌细胞凋亡的在研药物(Aguilar et al, J Med Chem 2017)。更多证据表明,APG-115激活p53也能促进肿瘤微环境中的抗肿瘤免疫(Fang et al, JITC 2019; Zhou et al, Nat Immunol 2021),但这些过程之间的关系尚未被完全了解。焦亡指的是炎性程序性细胞死亡。这一过程的核心是gasdermin家族蛋白,它可以在细胞膜上形成孔隙,导致免疫刺激物的裂解和释放。在表达这些蛋白的细胞中,GSDME可以被caspase-3切割,将非炎性细胞凋亡转化为焦亡(Zhang et al .,Nature 2020)。在这种情况下,caspase-3/GSDME代表了凋亡和焦亡之间的切换。鉴于大蒜素主要通过激活caspase-3来激发其凋亡活性,我们假设MDM2-p53抑制剂也可能通过裂解caspase来诱导GSDME阳性癌细胞的凋亡。
结论:
该研究表明,除细胞凋亡外,MDM2-p53抑制剂APG-115诱导caspase介导的GSDME阳性癌细胞焦亡。本研究首次揭示了APG-115在表达GSDME的癌细胞中能诱导细胞凋亡和焦亡。GSDME依赖性焦亡是APG-115除抗肿瘤免疫外的一种未被认识的作用机制,这对MDM2-p53抑制剂临床研究具有潜在的重要意义。
MDM2 inhibitor alrizomadlin (APG-115) stabilizes p53 and synergizes with proteasome inhibitors in multiple myeloma
MDM2抑制剂alrizomadlin (APG-115)可稳定多发性骨髓瘤中的p53并与蛋白酶体抑制剂产生协同作用
摘要编号:5439
研究背景:
在美国,多发性骨髓瘤(MM)约占所有肿瘤的2%和所有血液恶性肿瘤的18%。新开发的治疗方法(如免疫调节剂、蛋白酶体抑制剂、单克隆抗体)显著改善了治疗结果,但MM不可避免地复发,被认为是不可治愈的。基因组分析显示,TP53编码肿瘤抑制蛋白p53在MM患者中很少发生突变,这些患者中约有82%为TP53野生型。MDM2是一种可通过蛋白酶体降解抑制p53的E3泛素连接酶。蛋白酶体抑制剂可能有助于稳定p53并与MDM2抑制剂发挥协同作用。因此,可激活p53的MDM2抑制剂可能是治疗MM的一种有吸引力的药物。APG-115是一款作用于p53/MDM2相互作用的在研新型小分子药物,目前正在接受用于治疗实体瘤和血液肿瘤的临床开发。本研究旨在评估APG-115是否能增强蛋白酶体抑制剂在MM中的抗肿瘤作用。
上一篇:国产首款抗癌硼药,预计明年应用临床!价格约
下一篇:没有了