
《世界临床药物》

近年来,多款罕见病药物获批上市,并通过谈判纳入国家医保目录,这在解决患者药物支付问题的同时,也将进一步鼓励药企的创新投入。
在第十五个国际罕见病日之际,沙利文联合病痛挑战基金会于27日发布《2022中国罕见病行业趋势观察报告》(下称《报告》)。《报告》从罕见病药物研发、供给保障、资本投入、综合服务体系等角度研判趋势,药物研发则是其中重点。
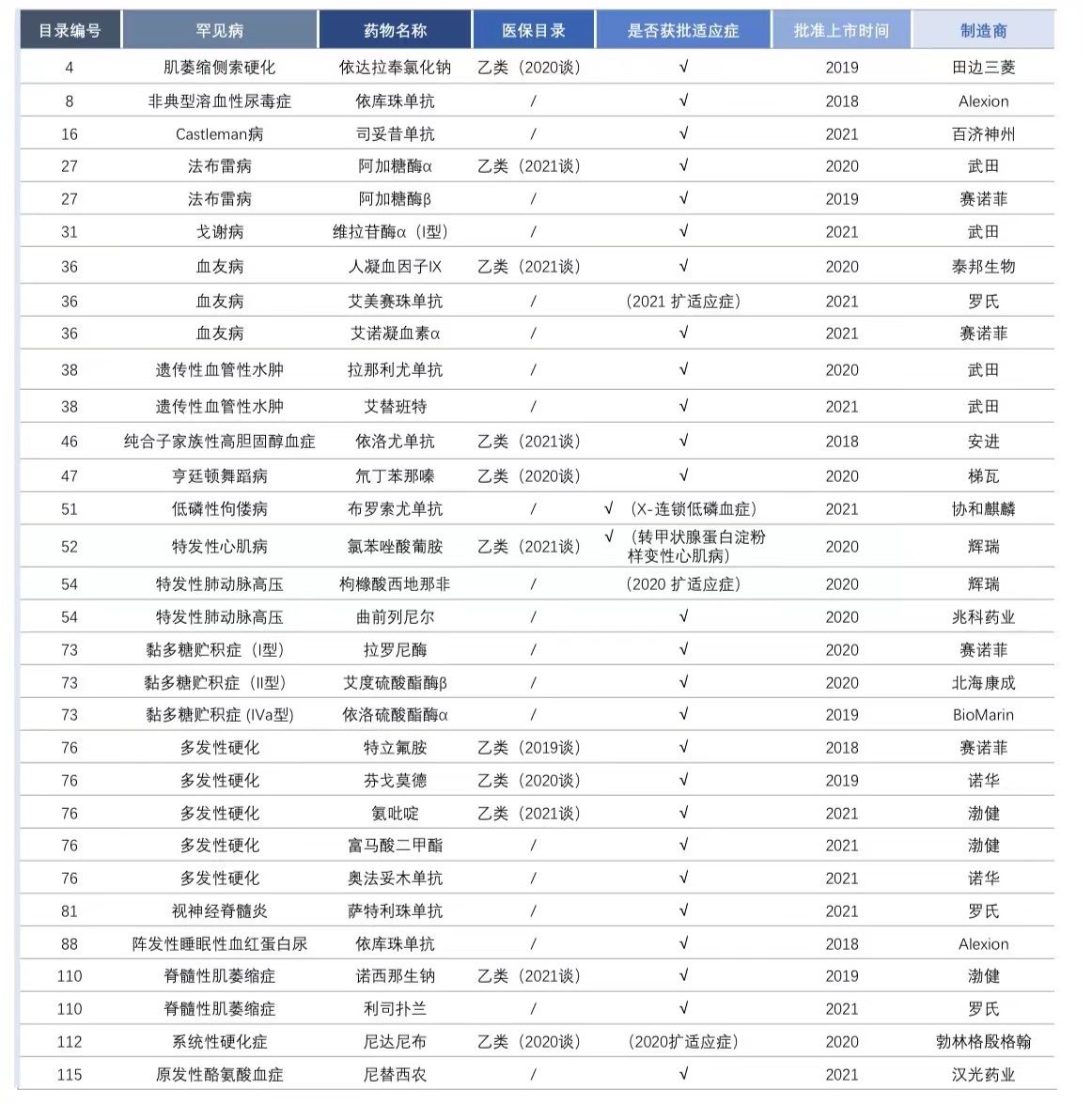
图为2018年罕见病目录发布后的上市的罕见病药物,数据来源:NMPA、国家及各地医保局
根据《报告》显示,罕见病药物的临床研发成功率较其他疾病药物要更高,这将进一步鼓励药企做创新投入。
详细来看,临床I期到II期罕见病药物的成功率为67%,所有疾病药物为52%,临床II期到III期罕见病药物的成功率为44.6%,而所有疾病药物为28.9%。
而从研发到上市全周期来看,罕见病药物临床I期到获批的成功率17%,而所有疾病的研发成功率为 7.9%,仅为罕见病药物的一半。
为此,沙利文大中华区合伙人兼董事总经理毛化在接受第一财经采访时表示,罕见病药物临床研发成功率的提升,一方面意味着各药企对于罕见病发病机理的探索、基础研究更加重视,另一方面,诸如基因疗法等新兴技术等,也在配合罕见病发病机理研究层面提供了有力支撑,并加快了研发进程。
《报告》还称,顶层利好政策为药企战略布局提供方向。比如,境外罕见病药物可通过纳入“临床急需”或经CDE(国家药监局药品审评中心)评估满足安全有效且无种族差异的要求,从而豁免临床试验;这些都大大缩短了境外罕见病新药在国内的上市时间,提升了药企引进罕见病新药的积极性。
《报告》还显示,除自主研发,企业还趋向于引进境外临床II~III期的项目来布局产品管线。比如,专注于罕见病领域的生物医药公司北海康成,拥有针对部分患者人数较多的罕见疾病以及罕见肿瘤适应症的13个创新产品管线,其中3 个产品已上市、4个产品已经进入临床试验阶段;曙方医药也在今年1月宣布与Santhera制药达成合作,获得罕见病新药Vamorolone在大中华区开发和商业化权益。
毛化告诉记者,对于有明确适应症的药物,国内药企目前还是会以原研为主,很少会去做仿制药;这是因为许多罕见病尚缺乏有明确适应症治疗药物,大多正处于研发中,国内药企有机会脱颖而出,况且我国还为创新药开设上市绿色通道。而对于已在全球获批的药物,其仍有较长的专利保护期,未来,国内药企也可以通过引进境外药物来实现患者的可及性。
上一篇:全球共3种药物可治胶质瘤,涉恒瑞医药、双鹭药
下一篇:没有了